2025年5月19日,《自然?衰老》期刊在線發表了題為《靶向染色質重塑物BAZ2B減輕肝衰老和MASH纖維化》的研究論文,該研究由中國科學院腦科學與智能技術卓越創新中心(神經科學研究所)蔡時青研究組與復旦大學公共衛生中心涂傳濤研究組合作完成,首次揭示表觀遺傳調控因子BAZ2B在肝臟衰老及代謝功能障礙相關性脂肪肝炎(MASH)纖維化中的關鍵作用,為開發新型治療策略奠定理論基礎。
MASH作為全球最普遍的慢性肝性疾病,可逐步發展為肝硬化、肝癌,是全球肝病死亡及肝移植的首要誘因。MASH在65歲以上人群中發病率激增,已成為老齡化社會的重大健康威脅。近年研究發現,肝臟衰老細胞在MASH纖維化進程中扮演"推手"角色,然而衰老如何驅動MASH疾病進展的分子機制并不清楚。
表觀遺傳在衰老相關MASH疾病進展中發揮重要作用,表觀遺傳調控如同基因表達的“編程開關”,環境壓力導致的染色質結構異常可能是MASH疾病的核心機制。蔡時青團隊前期工作(Nature 2020)發現一種重要的表觀調控分子——BAZ2B(BRD adjacent to zinc finger domain protein 2B),在衰老過程中其表達量顯著增加,抑制線粒體功能,妨礙大腦的健康老化并促進體重增加。
在本項研究中,蔡時青研究組與涂傳濤研究組合作,通過深入研究揭示了BAZ2B在衰老相關MASH疾病進程中的重要作用:在MASH患者肝臟活檢組織中,BAZ2B表達水平與脂肪變性及纖維化程度呈顯著正相關。全身敲除BAZ2B可顯著改善衰老小鼠及MASH模型小鼠的肝臟脂肪沉積、炎癥反應及纖維化,并逆轉細胞衰老表型。在分子機制上,BAZ2B通過結合糖脂代謝基因(如PPAR通路相關基因)啟動子區域,降低染色質可及性,抑制代謝調控網絡活性;而敲除BAZ2B可使衰老肝細胞"重煥活力",激活PPAR信號通路,重塑肝臟代謝穩態。在年輕及老年小鼠中,肝細胞特異性敲低BAZ2B均能有效阻斷MASH飲食誘導的病理進程,證實其作為治療靶點的可行性。這些發現表明,通過靶向BAZ2B使染色質結構恢復活力是減輕肝臟細胞衰老和纖維化的潛在策略。
全面認識衰老與慢性肝病之間的復雜聯系顯然具有重要意義。逆轉肝臟細胞衰老是預防和治療包括MASH在內的慢性疾病的潛在途徑。本研究首次構建BAZ2B-PPAR-脂質代謝軸這一連接表觀遺傳、衰老與肝纖維化的關鍵通路,為開發靶向染色質重塑的抗衰老療法提供全新方向。基于BAZ2B小分子抑制劑或基因編輯技術的臨床轉化研究已納入團隊下一步計劃。
該項工作由博士后錢程、李舒宇、劉至洋、林德穎,博士研究生歐陽皖贛、陳方圓,在蔡時青研究員與涂傳濤教授的指導下完成,腦智卓越中心蔡時青研究組的康心蕾以及復旦大學公共衛生學院宋舒等其他成員積極參與,并得到了腦智卓越中心實驗動物平臺、分子細胞技術平臺和光學成像平臺的大力支持。該工作得到國家自然科學基金委員會、科技部、中國科學院和上海市項目的資助。
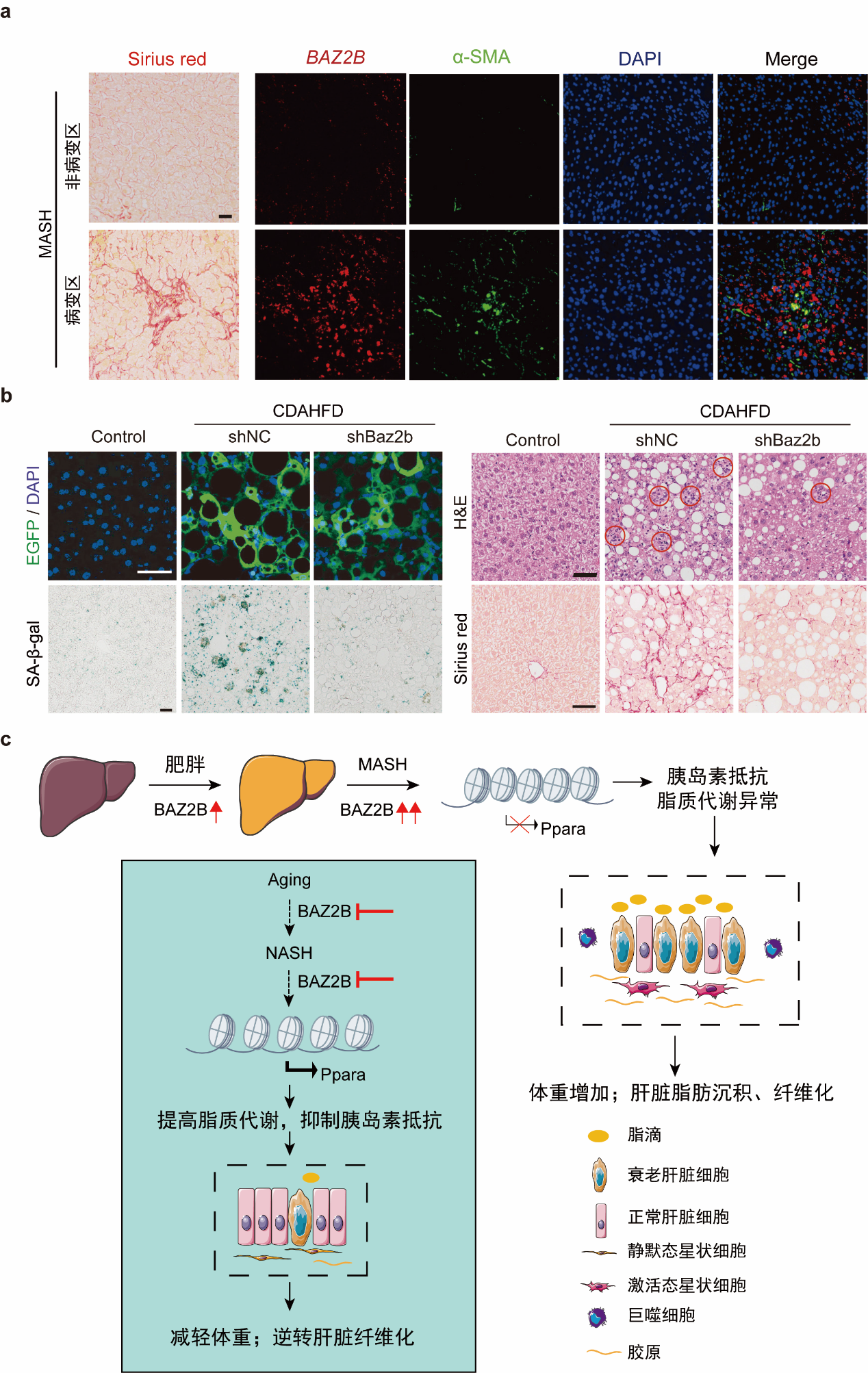
圖注: a, BAZ2B在MASH患者肝臟內表達的典型圖片,標尺等于50微米。b, TBG驅動EGFP在幼齡(2-3月齡)MASH小鼠肝臟中表達,以及SA-β-gal、 H&E、和天狼星紅染色的代表性圖像。MASH小鼠通過使用缺乏膽堿、 L-氨基酸限定的高脂肪飲食(CDAHFD)飼養8周造模。標尺,50 μm。c, BAZ2B參與調控肝臟衰老和MASH纖維化的模式工作圖。

 主站蜘蛛池模板:
河池市|
买车|
云梦县|
鲜城|
阳信县|
安龙县|
兰坪|
庆城县|
元谋县|
深圳市|
华亭县|
巴林左旗|
宜兰县|
安顺市|
赞皇县|
武隆县|
湾仔区|
盐津县|
盈江县|
亳州市|
英山县|
江阴市|
宁都县|
营口市|
盱眙县|
霍林郭勒市|
静海县|
青神县|
六安市|
桦南县|
敦煌市|
刚察县|
香港
|
土默特右旗|
原平市|
古蔺县|
龙川县|
马尔康县|
东兰县|
浠水县|
伊金霍洛旗|
主站蜘蛛池模板:
河池市|
买车|
云梦县|
鲜城|
阳信县|
安龙县|
兰坪|
庆城县|
元谋县|
深圳市|
华亭县|
巴林左旗|
宜兰县|
安顺市|
赞皇县|
武隆县|
湾仔区|
盐津县|
盈江县|
亳州市|
英山县|
江阴市|
宁都县|
营口市|
盱眙县|
霍林郭勒市|
静海县|
青神县|
六安市|
桦南县|
敦煌市|
刚察县|
香港
|
土默特右旗|
原平市|
古蔺县|
龙川县|
马尔康县|
东兰县|
浠水县|
伊金霍洛旗|